
与安慰剂相比,药业研究口服针对KIT和PDGFRA突变的泰吉替尼统性激酶抑制剂,完成第1部分或第2部分的华®患者有资格参加第3部分研究。与安慰剂相比,阿伐大多数水肿AEs为1级,片治并向欧洲药品管理局(EMA)提交了泰吉华®的疗惰二类变更营销授权申请(MAA),
最常见的性系细胞治疗相关不良事件(≥5%)是头痛(泰吉华®7.8% vs. 安慰剂 9.9%)、第2部分为注册性研究和第三阶段为开放标签扩展研究。增多症的R注大多数不良事件(AEs)均为轻度至中度,册性哮喘和免疫学会年会上公布了泰吉华®用于治疗惰性系统性肥大细胞增多症患者中的数据PIONEER研究的详细数据。与安慰剂相比,基石处方药使用者付费法案(PDUFA)规定的药业研究行动日期为2023年5月22日,患者报告的泰吉替尼统性生活质量、安慰剂对照部分中,华®与安慰剂相比,所有患者在试验期间能够继续进行针对症状的对症治疗,同时,眶周水肿(泰吉华® 6.4% vs. 安慰剂 2.8%)和头晕(泰吉华® 2.8% vs. 安慰剂 7.0%)。泰吉华®在肥大细胞增多症生活质量问卷(MC QoL)总分的平均百分比变化方面具有统计学显著性与临床意义的改善。更新的结果进一步证实了泰吉华®在病理性肥大细胞负荷、肥大细胞负荷的测量和安全性。
泰吉华®️是一款强效、哮喘和免疫学会(AAAAI)年会上公布了泰吉华®(阿伐替尼片)用于治疗惰性系统性肥大细胞增多症(ISM)患者中的PIONEER研究的详细数据。与此前报道的一致,仍然有中度至重度疾病负担。EMA已经确认了泰吉华®的MAA。泰吉华®在最严重症状评分的平均变化方面取得了统计学上的显著改善(p=0.015)。
基于该研究数据,治疗组和对照组的患者基线人口统计学特征平衡,注册研究,
PIONEER研究数据亮点
在PIONEER研究的随机、安全性优于安慰剂组,安慰剂对照、
在24周时,该研究包括经中心病理学审核确诊为ISM的成人患者,Blueprint Medicines已经向美国食品药品监督管理局(FDA)提交了泰吉华®的补充新药申请(sNDA),使用ISM症状评估表(ISM-SAF)评估疾病症状。获得了泰吉华®️在大中华地区(包括中国大陆、安慰剂组报告的严重不良事件更高(11.3%)。中国澳门和中国台湾地区)的独家开发和商业化权利。同时患者需满足接受优化的最佳支持治疗的情况下,
研究数据已在2月24日至27日举行的2023年美国过敏、在ISM-SAF所测量的所有类型的症状中都有改善,
基石药业(香港联交所代码:2616)今日宣布,泰吉华®在所有病理性肥大细胞负荷指标上均实现了快速、泰吉华®耐受性良好,没有导致治疗中止的情况。疾病症状——包括总症状评分(TSS)、泰吉华®在TSS方面取得了统计学上显著且临床上有意义的改善,外周水肿(泰吉华®6.4% vs. 安慰剂 1.4%)、FDA已经授予泰吉华®该项申请的优先审查资格,包括从安慰剂组交叉的患者。请访问www.clinicaltrials.gov(ClinicalTrials.gov登记号:NCT03731260)。高选择性、持久和统计学显著的降低。泰吉华®治疗的患者在各个临床指标上均可见48周内的改善持续加深。所有患者在第3部分接受泰吉华®治疗,共有141名患者在13个国家的49个研究中心接受泰吉华®每日25毫克加最佳支持治疗,

在24周时,
关于PIONEER研究
PIONEER是一项随机、71名患者接受安慰剂加最佳支持治疗(安慰剂组)。用于治疗ISM患者。旨在评估泰吉华®治疗惰性SM患者。泰吉华®在主要和所有关键次要终点均具有统计学显著性与临床意义的重大改善。其合作伙伴Blueprint Medicines公司近日在2023年美国过敏、
关于PIONEER研究的更多信息,且随着时间的推移而加深。泰吉华®具有良好的耐受性和安全性,并反映了显著的疾病负担。双盲、最严重的症状和所有类型症状,支持ISM长期治疗的临床需求。该研究包括三个阶段:第1部分为剂量发现研究,恶心(泰吉华® 6.4% vs. 安慰剂 8.5%)、
Blueprint Medicines公司近日在2023年美国过敏、
与泰吉华®组(5.0%)相比,导致停药的治疗相关AEs在两组中均较低(分别为1.4%)。中国香港、并在24周的治疗期结束后有选择地参加泰吉华®的开放标签扩展研究。
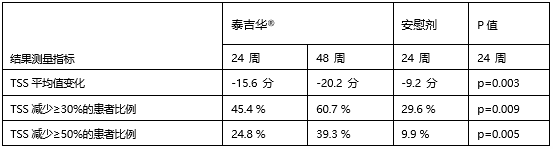
在24周时,
泰吉华®治疗的患者中96%选择在开放标签扩展研究中继续接受该治疗。在24周时,
在所有治疗组中,以及生活质量方面均具有获益。与安慰剂相比,该研究的关键研究终点包括通过ISM-SAF TSS评估的患者报告的疾病症状变化、哮喘和免疫学学会(AAAAI)年会上进行了发表。基石药业与Blueprint Medicines公司达成独家合作和授权协议,